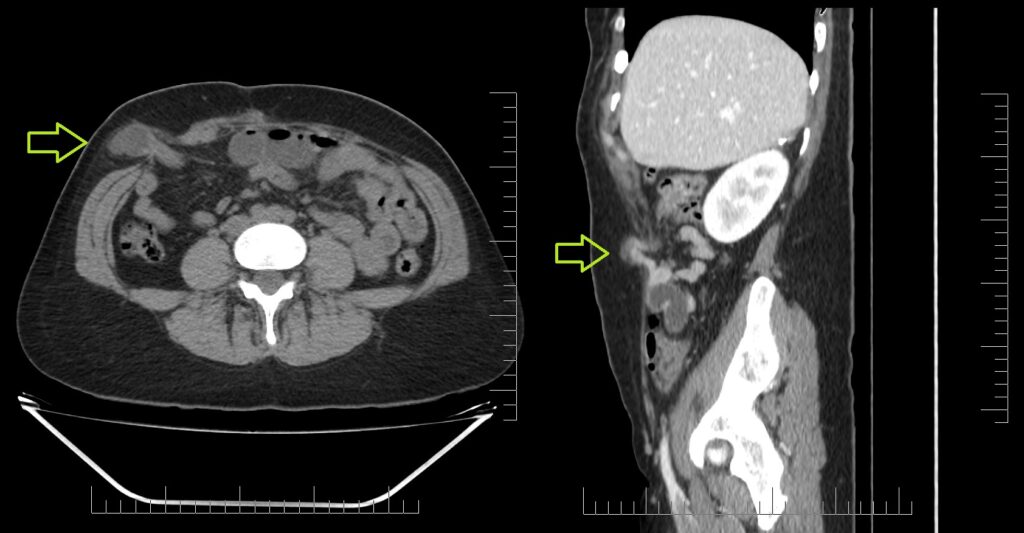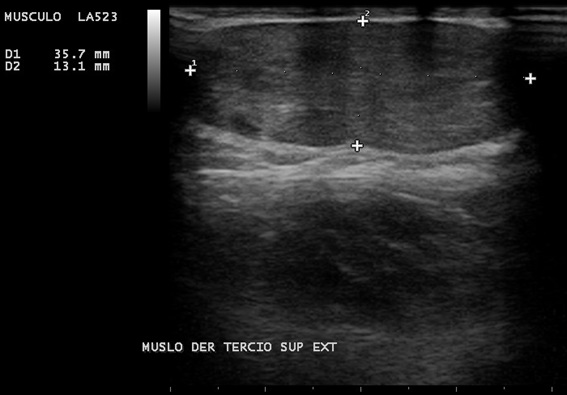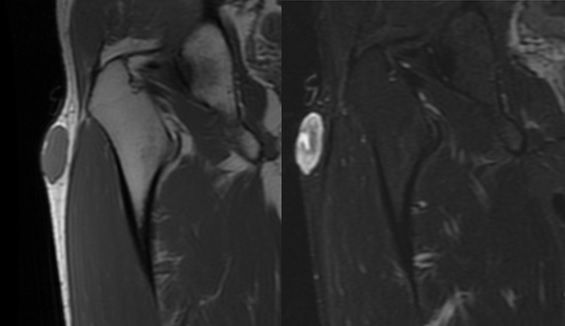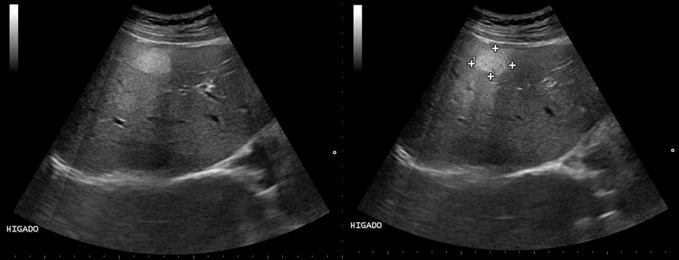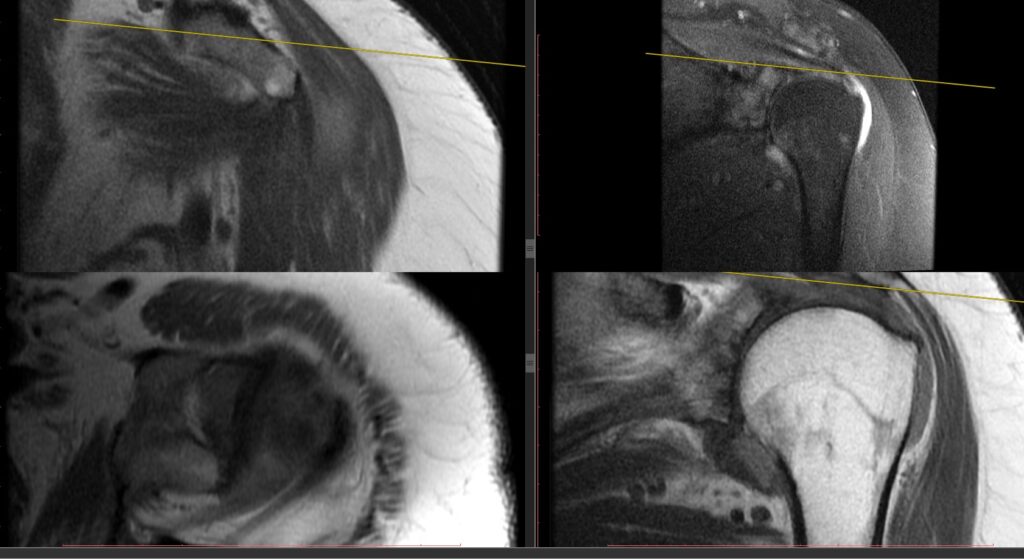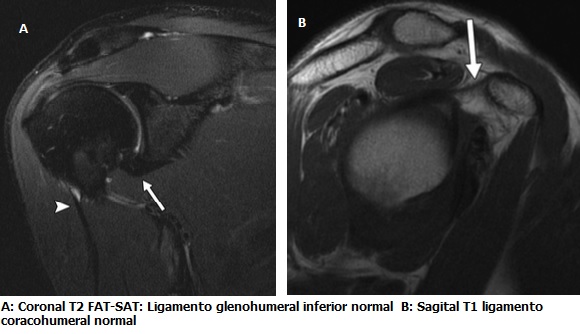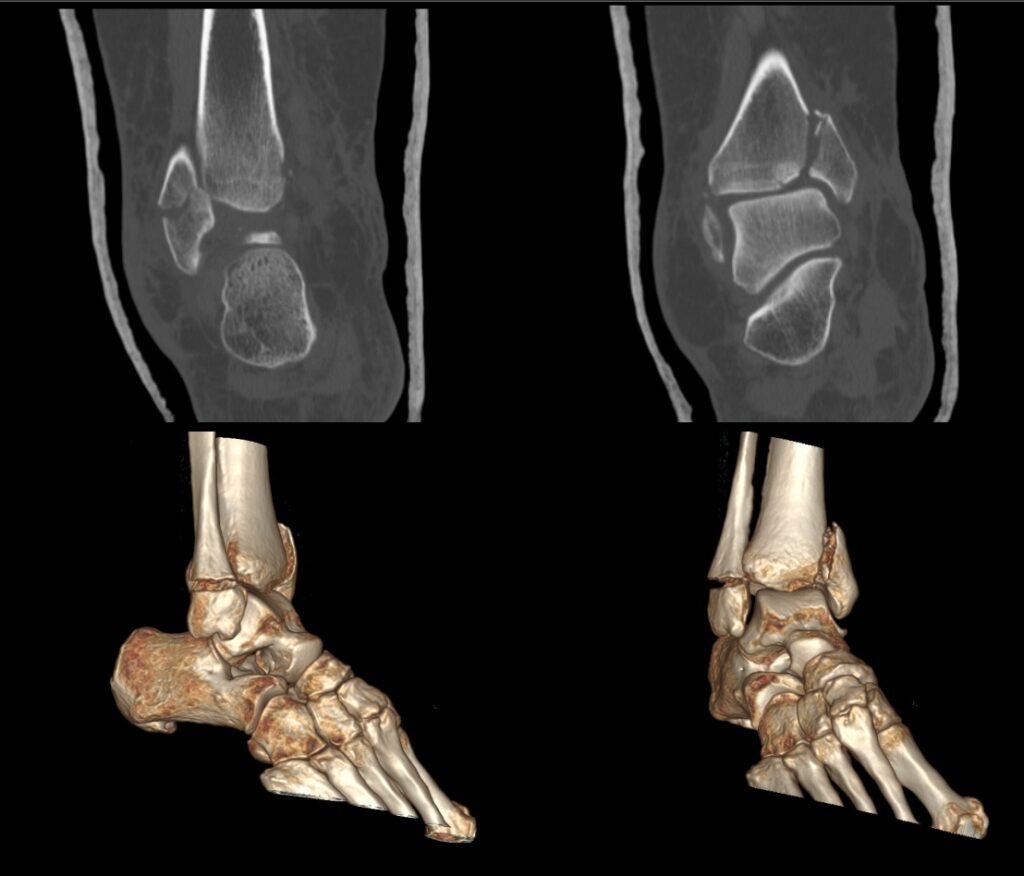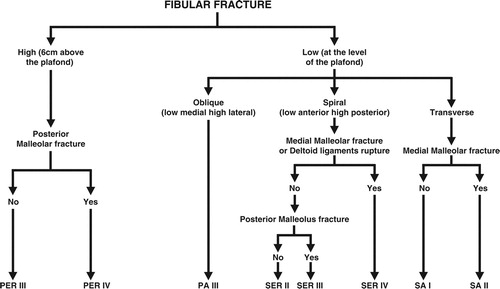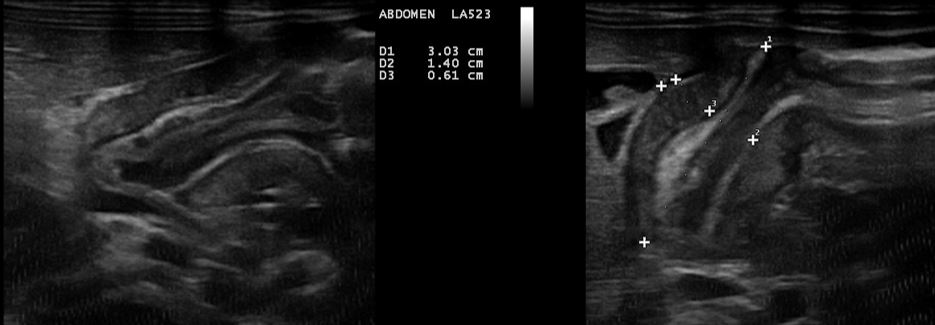
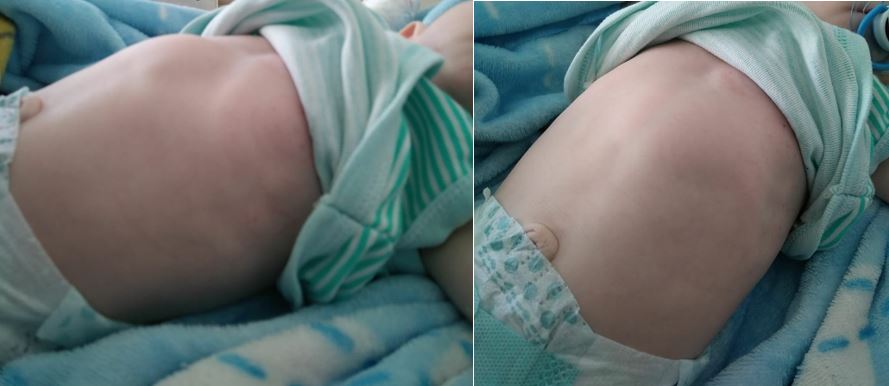
Paciente de 3 meses de edad, que inicia con emesis en multiples episodios al cumplir un mes de edad, cuadro que persistio en el tiempo, acompañado por perdida de peso progresiva y deshidratacion.
[expander_maker id=»1″ more=»Leer más» less=»Leer menos»]
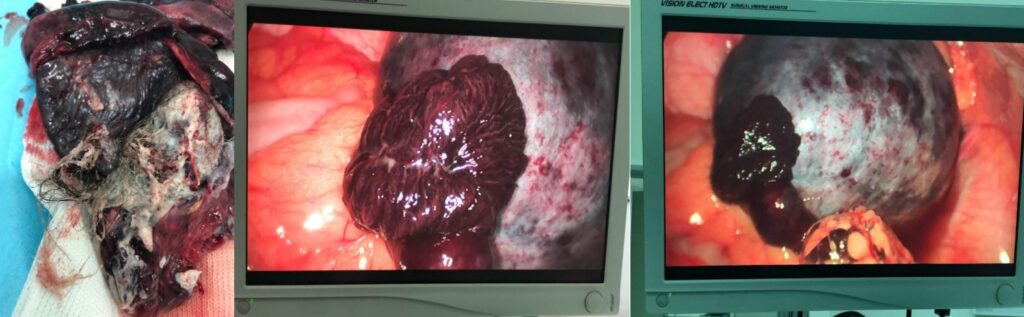
Diagnóstico: Estenosis pilórica hipertrófica infantil.
La estenosis pilórica hipertrófica infantil es una afección en la cual la porción antro pilórica del estómago presenta un engrosamiento anormal caracterizado por engrosamiento muscular y mucosa redundante lo cual genera una obstrucción al vaciamiento gástrico, con vómitos en proyectil, de carácter no bilioso, la frecuencia de vómitos aumenta hasta seguir a todas las alimentaciones. conduce a la deshidratación, la emaciación y en caso de no realizar tratamiento la muerte.
Incidencia de aproximadamente dos a cinco por 1.000 nacimientos por año.
La obstrucción funcional se desarrolla en las primeras 2 a 12 semanas de vida.
La evaluación ecográfica al nacer evidencia anatomía normal.
Claves para el diagnóstico:
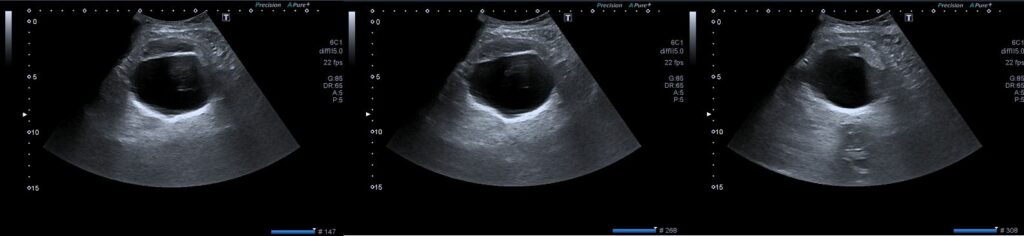
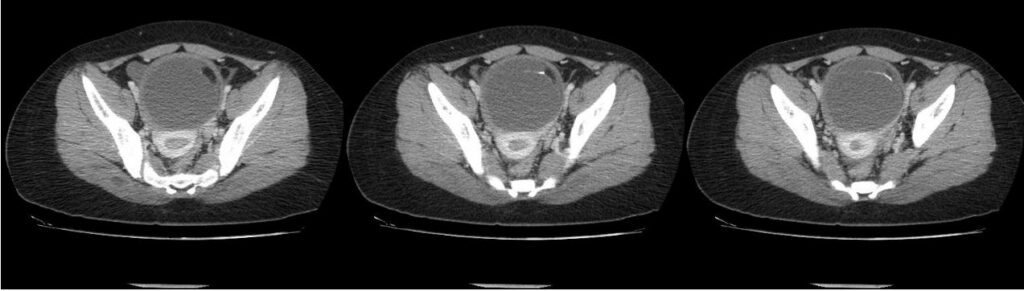
Ecografía: El examen debe realizarse con transductor lineal de alta frecuencia entre 6 y 10 MHz, con un posicionamiento adecuado del paciente.
En la ecografía se puede observar el antro prepilórico engrosado que une el bulbo duodenal y el estómago el cual se encontrara distendido. Esta distensión de la cámara gástrica en un niño que presenta vomito a repetición es el primer signo disponible para pensar que hay una obstrucción de la salida gástrica.
Como hallazgos ecográficos directos se evidencia engrosamiento del músculo pilórico hipertrofiado el cual es hipoecoico, con una mucosa central redundante e hiperecogenica.
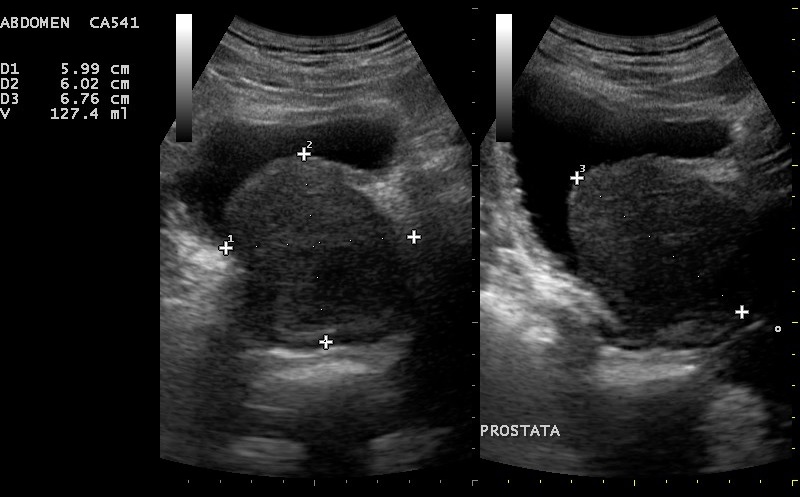
Se realizan medidas del grosor del músculo pilórico, es decir, el diámetro de una sola pared muscular (componente hipoecoico) en una imagen transversal la cual mida más de 3 mm.
Diámetro pilórico transversal mayor 14 mm
El diámetro longitudinal mayor a 16mm.
Diagnostico Diferencial
Piloroespasmo.
Malrotación Intestinal.
Hernia de hiato.
Estenosis duodenal preampular.
Bibliografía:
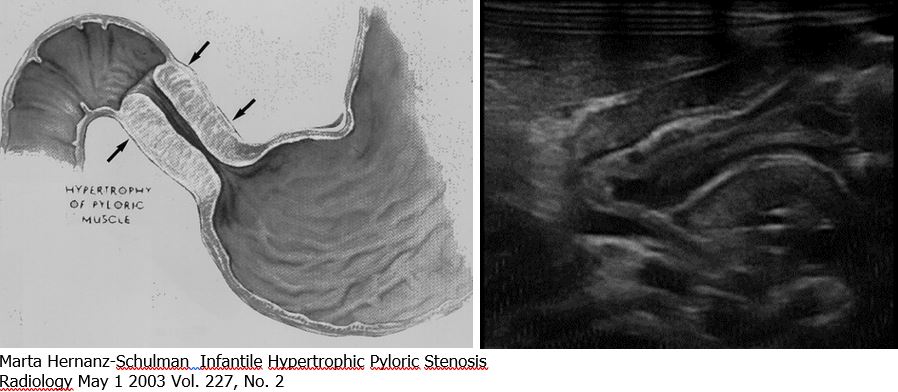
Marta Hernanz-Schulman Infantile Hypertrophic Pyloric Stenosis,
Radiology May 1 2003 Vol. 227, No. 2
Marta Hernanz-Schulman, Yuwei Zhu, Sharon M. Stein, Richard M. Heller, L. Allison Bethel, Hypertrophic Pyloric Stenosis in Infants: US Evaluation of Vascularity of the Pyloric Canal, Radiology Nov 1 2003 Vol. 229, No. 2
[/expander_maker]